Pipeline
La pipeline attuale di BIOGENERA SpA rispecchia il forte impegno dell’azienda nella ricerca in aree altamente specialistiche e ad elevata necessità medica: i tumori e le malattie metaboliche e dermatologiche. BIOGENERA SpA sta infatti sviluppando molteplici molecole gene-specifiche in grado di rivoluzionare le cure e la vita dei pazienti.

Oncologia
| Farmaco | Gene target | Patologia | Ricerca | Studi preclinici | Fase I | Fase II | Fase III |
|---|---|---|---|---|---|---|---|
| BGA002 | MYCN | Tumori MYCN positivi | |||||
| BGA003 | MYC | Tumori MYC positivi | |||||
| BGA005 | Survivin | Tumori Survivin positivi | |||||
| BGA006 | ALK | Tumori ALK positivi | |||||
| BGA007 | PLK4 | Tumori PLK4 positivi | |||||
| BGA008 | BCL2 | Tumori BCL2 positivi |
Dermatologia e malattie metaboliche
| Farmaco | Gene target | Patologia | Ricerca | Studi preclinici | Fase I | Fase II | Fase III |
|---|---|---|---|---|---|---|---|
| BGA011 | Pelle | Bersaglio terapeutico confidenziale | |||||
| BGA012 | Disordine metabolico | Bersaglio terapeutico confidenziale |
I tumori MYCN
I tumori MYCN positivi, caratterizzati da una prognosi sfavorevole, hanno un’incidenza del 25% sulla totalità dei tumori, ma raggiungono quota 50% nei tumori pediatrici.

Incidenza MYCN sulla totalità dei tumori
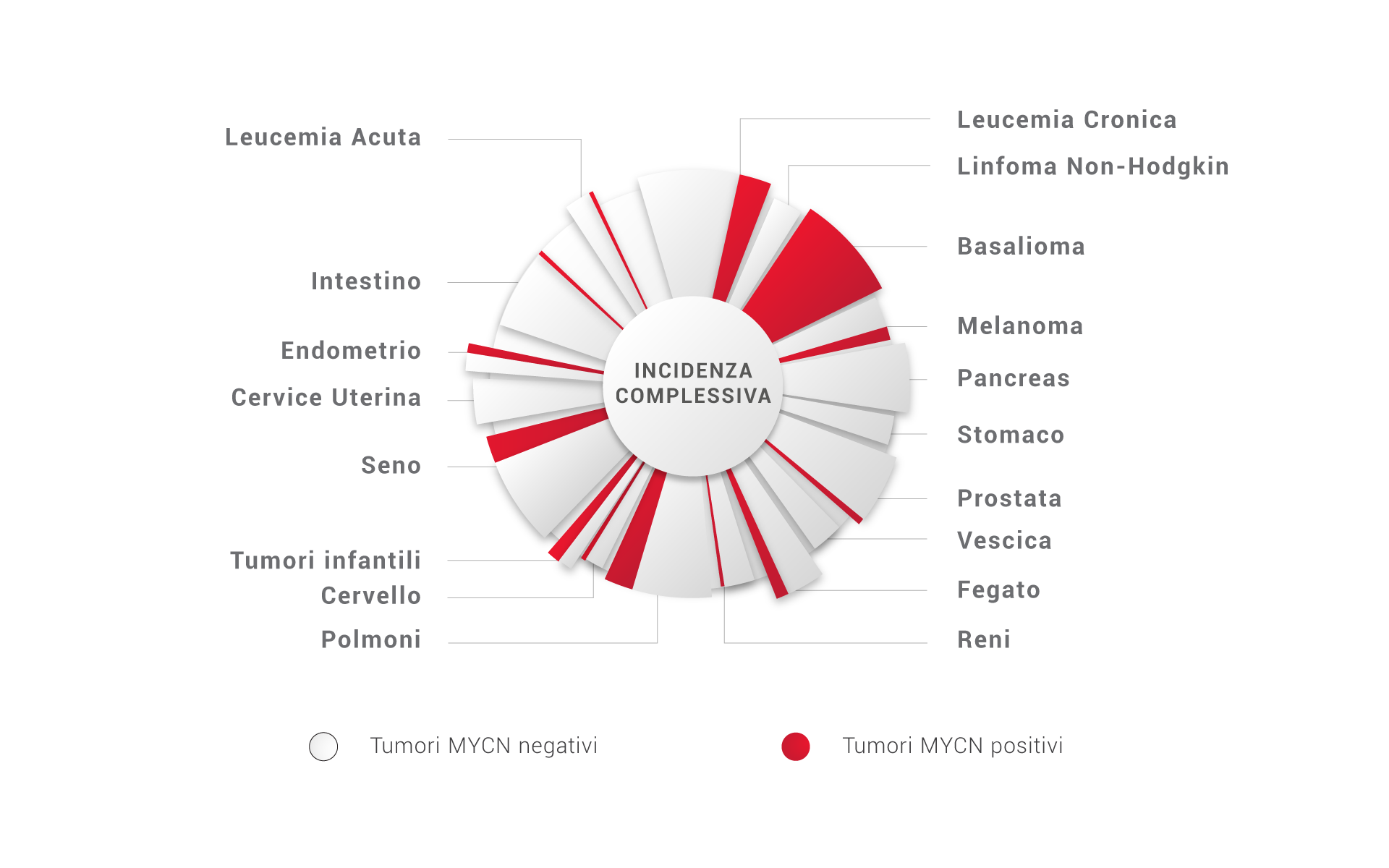
Incidenza MYCN sui tumori pediatrici

Il primo utilizzo di BGA002
il Neuroblastoma

BIOGENERA SpA ha concluso gli studi preclinici di BGA002, il primo ed unico farmaco a livello internazionale con azione diretta e specifica per il blocco del gene tumorale MYCN, per il trattamento dei tumori MYCN positivi.
Tra questi è incluso il Neuroblastoma, il tumore pediatrico maligno che è la prima causa di morte per tumore nei bambini al di sotto dei 15 anni (15% del totale dei decessi).
L’obiettivo attuale è effettuare gli studi di Fase I, ma un primo importante traguardo è già stato raggiunto: il farmaco BGA002 ha ottenuto la designazione di farmaco orfano per il Neuroblastoma dall’Agenzia Europea dei Medicinali (EMA) e dalla Food and Drug Administration (FDA) degli USA, e per il gruppo dei sarcomi delle parti molli (dall’EMA), il che consentirà di velocizzare l’iter di sviluppo e quindi fornire ai pazienti un’alternativa terapeutica concreta.
Inoltre, il farmaco BGA002 ha gia’ ottenuto anche la “Rare Pediatric Designation” dalla Food and Drug Administration (FDA) degli USA per il Neuroblastoma. BGA002 è sviluppato anche per altri gravi tumori pediatrici MYCN positivi. Inoltre il farmaco BGA002 è sviluppato anche per gravi tumori MCYN positivi dell’adulto, nell’ambito dei quali il farmaco BGA002 ha gia´ottenuto la designazione di fármaco orfano dall’FDA per il trattamento del tumore del polmone a piccole cellule (Microcitoma), il tumore al polmone piu’ mortale ed il piu’ associato al fumo.

BIOGENERA SpA ha concluso gli studi preclinici di BGA002, il primo ed unico farmaco a livello internazionale con azione diretta e specifica per il blocco del gene tumorale MYCN, per il trattamento dei tumori MYCN positivi.
Tra questi è incluso il Neuroblastoma, il tumore pediatrico maligno che è la prima causa di morte per tumore nei bambini al di sotto dei 15 anni (15% del totale dei decessi).
L’obiettivo attuale è effettuare gli studi di Fase I, ma un primo importante traguardo è già stato raggiunto: il farmaco BGA002 ha ottenuto la designazione di farmaco orfano per il Neuroblastoma dall’Agenzia Europea dei Medicinali (EMA) e dalla Food and Drug Administration (FDA) degli USA, e per il gruppo dei sarcomi delle parti molli (dall’EMA), il che consentirà di velocizzare l’iter di sviluppo e quindi fornire ai pazienti un’alternativa terapeutica concreta.
Inoltre, il farmaco BGA002 ha gia’ ottenuto anche la “Rare Pediatric Designation” dalla Food and Drug Administration (FDA) degli USA per il Neuroblastoma. BGA002 è sviluppato anche per altri gravi tumori pediatrici MYCN positivi. Inoltre il farmaco BGA002 è sviluppato anche per gravi tumori MCYN positivi dell’adulto, nell’ambito dei quali il farmaco BGA002 ha gia´ottenuto la designazione di fármaco orfano dall’FDA per il trattamento del tumore del polmone a piccole cellule (Microcitoma), il tumore al polmone piu’ mortale ed il piu’ associato al fumo.

